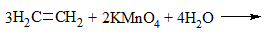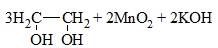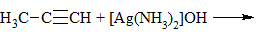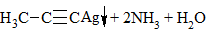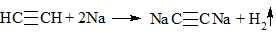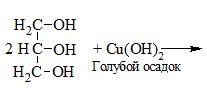С чем взаимодействует бромная вода в органике
Химия, Биология, подготовка к ГИА и ЕГЭ
Качественные реакции органической химии
В качественном анализе используют легко выполнимые, характерные химические реакции, при которых наблюдается появление или исчезновение окрашивания, выделение или растворение осадка, образование газа и др. Реакции должны быть как можно более селективны и высокочувствительны.
Итак, классы органических соединений и соответствующие им качественные реакции:
| Класс органических соединений | Качественные реакции |
| Алканы | У алканов нет качественных реакций. Их определяют методом исключения |
| Алкены | 1. Обесцвечивание бромной воды: 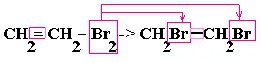 2. Изменение окраски раствора 2. Изменение окраски раствора3СH2=CH2 + 2 KMnO4 + 4H2O → 3C2H4(OH)2 + 2 MnO2 + 2KOH |
| Циклоалканы | Обесцвечивание бромной воды: 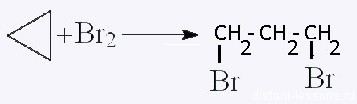 |
| Алкины | 1. Обесцвечивание бромной воды, 2. Образование ацетиленидов серебра и меди:  3. Изменение окраски перманганата калия: (KMnO4 → MnO2) C2H2 → HOOC-COOH |
| Алкадиены | Т.к. алкадиены содержат 2 двойные связи, то они так же как и алкены, обесцвечивают бромную воду |
| Арены | 1. Взаимодействие с бромом (в присутствии катализатора) 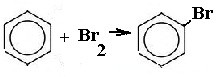
|
| Спирты | Реакция с оксидом меди — в осадок выпадает медь: 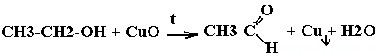 |
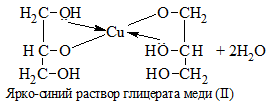
| Многоатомные спирты | С гидрокисдом меди (II) — Cu(OH)2 образуется комплекс синего цвета |
| Альдегиды | Реакция «серебряного зеркала» и реакция «медного зеркала»: 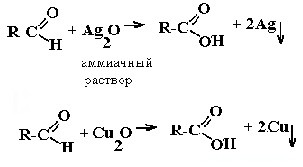 |
| Кислоты органические | Дают окрашенные соли тяжелых металлов — см. таблицу растворимости |
| Амины | Качественных реакций нет (только анилин — имеет характерный запах) |
Как вы видите, все вещества, имеющие кратные связи (кратные=двойные и тройные), обесцвечивают бромную воду. Многие из них изменяют окраску раствора перманганата калия. Поэтому эти вещества надо разделять по их индивидуальным, характерным только для них качественным реакциям.
Здесь перечислены самые основные качественные реакции органической химии. Если говорить о высокомолекулярных соединениях — белках, жирах, углеводах, то для них качественные реакции определяются функциональными группами, входящими в состав. Зная функциональную группу, вы легко сможете подобрать реактив, т.к. в таблице они разобраны именно по классам.
4.1.5. Качественные реакции органических соединений.
Алкены >C=C C=C C(OH)-C(OH) C=C C(Br)-C(Br) +
Постепенное обесцвечивание подкисленного раствора KMnO4. Выпадения бурого осадка MnO2 не наблюдается, поскольку марганец восстанавливается до практически бесцветной соли двухвалентного марганца. Чаще всего в качестве подкислителя изпользуют серную кислоту. На примере с толуолом реакция выглядит следующим образом:
Исчезновение желто-коричневой окраски бромной воды с одновременным выпадением белого осадка трибромфенола:
Разбавленный водный раствор соли железа (III), например,
Исчезновение желто-коричневой окраски бромной воды с одновременным выпадением белого осадка триброманилина:
Одноатомные первичные и вторичные спирты
R-CH2-OH + CuO =t o => R-CHO + Cu + H2O,
вторичный — в кетон:
R-C(OH)-R’+ CuO =t o => R-C(O)-R’ + Cu + H2O,
В случае метанола появляется легко узнаваемый запах формальдегида (естественно, чтобы он был узнаваемым, нужно до этого быть знакомым с его запахом:-) )
В случае реакции с CuO этилового спирта чувствуется специфический запах ацетальдегида, схожий с ароматом прелых яблок сорта «антоновка»
Растворение голубого осадка Cu(OH)2 с образование ярко-синего раствора комплексного соединения меди. На примере с глицерином уравнение реакции выглядит следующим образом:
Альдегиды,
—CHO
Аммиачный раствор оксида серебра
Так называемая реакция серебряного зеркала. В результате восстановления Ag +1 в металлическое серебро Ag 0 на стенках сосуда образуется зеркало. При небрежном смешении реагентов или в недостаточно чистом сосуде вместо серебряного зеркала может образоваться черный осадок, состоящий из мелкодисперсных частиц металлического серебра. В обоих случаях наблюдаемые явления описываются уравнением в общем виде:
Образование оранжево-красного осадка Cu2O при нагревании в результате реакции:
Карбоновые кислоты,
-COOH
Выделение углекислого газа в результате разложения образующейся нестойкой угольной кислоты H2CO3:
Появление запаха сложного эфира, образующегося в результате реакции:
R-COOH + R’-OH → R-COO-R’ + H2O
Запахи эфиров весьма разнообразны, но общим является ярко выраженная пахучесть, нередко, могут напоминать ароматы различных фруктов.
Муравиная кислота
-СООН
Окрашивание лакмуса в красный цвет, по причине кислой среды, создаваемой муравьиной кислотой:
Аммиачный раствор оксида серебра
Молекуле муравьиной кислоты, не смотря на ее малый размер удается сочетать в себе помимо карбоксильной группы также и карбонильную, которая позволяет вступать муравьиной кислоте в реакцию серебряного зеркала подобно альдегидам:
Растворимые соли жирных карб. кислот, например, стеарат натрия
Выпадение хлопьевидного белого осадка малорастворимой жирной кислоты:
Выпадение белого осадка нерастворимой кальциевой или магниевой соли жирной кислоты. Ионное уравнение в общем виде:
где R-длинный углеводородный радикал.
На примере, стеарата натрия и хлорида кальция молекулярное уравнение реакции выглядит так:
Окрашивание фенолфталеина в малиновый цвет как в щелочах, ввиду того, что соли жирных кислот гидролизуются по аниону:
Химические свойства брома, уравнения реакций
Общая характеристика
Данное вещество при нормальных условиях представляет собой красно-бурую жидкость. Она едкая, тяжелая, имеет неприятный запах, который немного напоминает йодный. Жидкость ядовитая, но про токсичные свойства химического элемента брома будет рассказано чуть позже. Общие характеристики можно выделить в следующий перечень:
Интересно, что название этого элемента с древнегреческого переводится как «зловоние». И кто знает, как пахнут бромовые растворы, понимает, о чем речь. Запах у него действительно не из приятных.
Основные химические свойства
Данное вещество существует в виде 2-атомных молекул Br2. Если увеличить температуру до 800 °C, то станет заметна их диссоциация на атомы. Чем выше будут градусы, тем интенсивнее будет осуществляться данный процесс.
К основным химическим свойствам брома стоит отнести его способность растворяться в воде. Это, конечно, характерно для всех галогенов, но он лучше остальных взаимодействует с Н2О. Растворимость составляет 3,58 грамм на 100 миллилитров воды при температуре в 20 °C.
Получающийся в итоге этой реакции раствор именуют бромной водой. У нее есть целый ряд специфических особенностей.
Бромная вода
На свету она постепенно выделяет кислород. Это возникает из-за того, что бромноватистая кислота, входящая в состав данного раствора, начинает разлагаться. Жидкость, кстати, имеет характерный желто-оранжевый цвет.
Бромную воду используют для проведения реакции, которая в виде формулы выглядит так: Br2 + Н2О → HBr + HBrO. Как можно видеть, в результате образуются такие вещества, как бромоводородная и неустойчивая бромноватистая кислоты.
А готовят ее обычно так: в 250 миллилитров дистиллированной воды добавляют бром в количестве 1 мл, интенсивно при этом перемешивая компоненты. Процесс осуществляется в вытяжном шкафу. Хранят раствор в емкости, выполненной из стекла темного цвета.
Другие реакции брома
Важно оговориться, что этот активный неметалл во всех отношениях смешивается с большинством органических растворителей. Чаще всего вследствие данного процесса их молекулы бромируются.
По своей химической активности данный элемент находится между хлором и иодом. С этими веществами он тоже взаимодействует. Вот, например, реакция с раствором иодида, вследствие которой образуется свободный иод: Br2 + 2Kl → I2 + 2KBr. А при воздействии на бромиды хлора появляется свободный бром: Cl2 + 2KBr → Br2 + 2KCl.
Со многими другими веществами рассматриваемый элемент тоже взаимодействует за счет своих химических свойств. Реакция брома с серой дает S2Br2. При взаимодействии с фосфором появляются PBr3 и PBr5. Это все бинарные неорганические соединения. Кроме перечисленных элементов, неметалл также взаимодействует с селеном и теллуром.
И, конечно, рассказывая про физические и химические свойства брома, нельзя не упомянуть, что существуют также вещества, являющиеся устойчивыми к его действию. Это платина и тантал, а еще в какой-то мере свинец, титан и серебро.
Двойные и тройные связи
С веществами, которым они свойственны, также способен взаимодействовать обсуждаемый элемент. И, рассказывая про химические свойства брома, уравнения реакций данного типа тоже стоит рассмотреть. Вот одно из таковых: С2Н4 + Br2 → C2H4BR2. Это взаимодействие с этиленом. Ему как раз и свойственна двойная связь.
Интересно, что когда бром смешивается с растворами щелочей, карбоната калия или натрия, то результатом становится образование соответствующих броматов и бромидов (солей). Вот уравнение, демонстрирующее это: 3Br2 + 3Na2CO3 → 5NaBr + NaBrO3 + 3СО2.
И да, перечисляя важнейшие химические свойства брома, нельзя не упомянуть, что в жидком состоянии он легко взаимодействует с золотом. Результатом становится образование трибромида (AuBr3). А реакция выглядит следующим образом: 2Au + 3Br2 → 2AuBr3.
Токсичность
Химические свойства брома обусловливают его опасность для человеческого организма. Даже если его концентрация в воздухе превышает отметку в 0,001 % по объему, то возникают головокружение, раздражение слизистых оболочек, кровотечение из носа, а иногда даже удушье и спазмы дыхательных путей.
Смертельная доза для человека составляет всего 14 мг/кг перорально. Если возникло отравление бромом, то нужно:
Бром действительно опасное вещество. Его даже используют в производстве боевых отравляющих припасов.
Работа с бромом
Поскольку химические свойства брома обусловливают его токсичность, то люди, которые вынуждены с ним контактировать, используют специальные перчатки, противогазы и спецодежду.
Хранят вещество в толстостенной таре из стекла. Ее, в свою очередь, хранят в емкостях с песком. Он помогает защитить тару от разрушения, которое может возникнуть из-за встряхивания.
Кстати, из-за очень высокой плотности вещества бутылки с ним нельзя брать за горло. Оно легко может оторваться. А последствия от разлитого токсичного брома, да еще в таком количестве, катастрофичны.
Применение
Напоследок пару слов о том, как и где используют бром. Можно выделить следующие сферы и области применения:
Так что каким бы токсичным ни было это вещество для человеческого организма, в некоторых сферах оно незаменимо.
Некоторые темы органической химии для подготовки к ЕГЭ
Задание 25. Качественные реакции (подробно)
1. Как распознать алкены и стирол (в случае стирола в реакции вступает только двойная связь боковой цепи, а не бензольное кольцо)
1) + Br2 (бромная вода) → обесцвечивание раствора (реакция протекает в обычных условиях)
2) + KMnO4 (водный раствор) → обесцвечивание раствора, образование осадка MnO2 бурого цвета:
Раствор перманганат калия фиолетового цвета. В результате реакции окраска исчезает, образуется осадок MnO2 бурого цвета.
2. Как распознать алкины
1) + Br2 (бромная вода) → обесцвечивание раствора (реакция протекает в обычных условиях):
3) + [Ag(NH3)2]OH → выпадение осадка в случае концевой тройной связи:
4) + Металл → выпадение осадка и выделение водорода в случае концевой тройной связи
3. Как распознать бензол
1) Бензол горит коптящим пламенем из-за большого содержания углерода.
Благодаря устойчивой ароматической системе бензол не вступает в реакции с водным раствором Br2 и раствором KMnO4.
4. Как распознать одноатомные спирты
1) + CuO → наблюдаем выделение металлической меди:
CH3-CH2-OH + CuO → CH3-CHO + Cu + H2O (t, окисление спиртов до альдегидов)
С основаниями одноатомные спирты не взаимодействуют.
5. Как распознать многоатомные спирты
1) + Cu(OH)2 → растворение голубого осадка и появление ярко-синей окраски раствора:
С щелочами многоатомные спирты не взаимодействуют.
6. Как распознать фенолы
1) + Br2 → выпадение белого осадка 2,4,6-трибромфенола
2) + FeCl3 → раствор фиолетового цвета
7. Как распознать альдегиды
1) + [Ag(NH3)2]OH → восстановление металлического серебра
2) + Cu(OH)2 → выпадение осадка Cu2O кирпично-красного цвета
8. Как распознать карбоновые кислоты
1) раствор лакмуса → изменение окраски на красную
2) + Na2CO3/NaHCO3  → выделение газа CO2
9. Как распознать соли высших карбоновых кислот
1) + HCl (любая сильная кислота) → появление хлопьев нерастворимых высших кислот
10. Как отличить муравьиную кислоту от уксусной
Муравьиная кислота содержит и альдегидную группу тоже, следовательно, возможны реакции, характерные альдегидам:
1) + [Ag(NH3)2]OH → восстановление металлического серебра и выделение газа (так как кислота окисляется до CO2)
2) + Cu(OH)2 → выпадение осадка Cu2O кирпично-красного цвета и выделение газа (так как кислота окисляется до CO2).
11. Как распознать низшие амины
1) раствор лакмуса → изменение окраски на синюю (так как среда раствора щелочная)
1) раствор фенолфталеина → изменение окраски на малиновую
12. Как распознать анилин
1) + Br2 → выпадение белого осадка 2,4,6-триброманилина
13. Как распознать белок
1) + HNO3 → желтое окрашивание (ксантопротеиновая реакция)
2) + Cu(OH)2 → фиолетовое окрашивание (биуретовая реакция)
14. Как распознать глюкозу C6H12O6
1) + Cu(OH)2 → растворение голубого осадка и появление ярко-синей окраски раствора (реакция на несколько гидроксильных групп)
2) + Cu(OH)2 → при нагревании образуется осадок Cu2O красного цвета (реакция на альдегидную группу)
3) + [Ag(NH3)2]OH → восстановление металлического серебра
15. Как распознать крахмал
1) + I2 → появление синей окраски.
Бромная вода: что это такое и чем опасна для человека, химическая формула брома, методы очистки, взаимодействие с другими веществами
Рассмотрим раствор, активно используемый в промышленности. В фокусе внимания – бромная вода: что это такое, состав, как выглядит, структурная химическая формула и свойства, чем опасен бром для человека – пройдемся по всем этим вопросам, чтобы вы имели полное представление.
Сразу отметим, что особенно важна и востребована оно в лабораториях, где используется для выявления алкенов, которые она идентифицирует, изменяя свой цвет. И развеем один старый миф: что ее якобы давали советским солдатам для снижения потенции. Вряд ли, потому что для этого не было поводов, она не уменьшает либидо и не оказывает отрицательного влияния на мужскую силу. Если ее и подливали в напитки, то лишь в качестве мягкого снотворного, хотя и этому нет никаких доказательств. Ну а теперь сосредоточимся на более специфических моментах.
Определение
Это раствор, состав которого можно записать по схеме:
«бром плюс вода и кислоты» (бромоводородная и бромноватистая)
В обычных условиях это желто-оранжевая по своему цвету жидкость с высокой степенью прозрачности. Является достаточно активным веществом, успешно сочетающимся как с органикой, так и с неорганическими соединениями. Довольно сильный окислитель, быстро воздействующий в щелочной среде на катионы Mn+3, Ni+3, Cr+3, Co+2, Fe+2, а также в отдельном порядке на фенолы.
Формула
Записывается максимально просто – Br2, – не только соответствуя встречающейся в природе молекуле элемента, но и отражая ее количественный и качественный состав.
Но также содержит HBr и HBrO, которые тоже заслуживают внимания, так как определяют особенности хранения. За счет наличия этих свободных кислот значительно снижает pH-уровень той технологической среды, в которую добавлена (и эта ее особенность имеет ключевое значение при фильтрации, естественно, при соблюдении должной дозировки). И является важным компонентом при проведении целого ряда анализов и при изготовлении многих органических препаратов.
Формула бромной воды в химии
Br2 позволяет определить молекулярную массу – из следующих уравнений:
Mr(Br2) = 2 х Ar(Br), то есть Mr(Br2) = 2 х 80 = 160
Одна из наиболее частых реакций:
Br2 + H2O ⇌ HBr + HBrO
Если развернуть это описание и осветить его более подробно, система уравнений приобретет вид:
Br2(K) + nH2O ⇌ Br2 x nH2O(P),
что, в свою очередь, можно преобразовать в:
Br2 x nH2O ⇌ HBr + HBrO + (n – 1) x H2O,
из этого вырастает:
HBrO + H2O ⇌ BrO- + H3O+
К тому, как взаимодействуют оксид брома и вода, нужно добавить, что массовая доля элемента в составе в норме не превышает 3,5%, но при наличии бромидов степень растворимости увеличится благодаря появлению следующих комплексов:
которые подвергаются постепенному разложению под воздействием света:
1,5 м3/ч Для технической воды
1,5 м3/ч Для технической воды
MBFT-75 Мембрана на 75GPD
Последний процесс запускает бромноватистая кислота и, чтобы его предупредить, следует держать вещество в затемненной таре или хотя бы не подвергать его воздействию прямых лучей. При должном хранении с соблюдением всех норм оно сбережет свои полезные в условиях лаборатории свойства в течение долгого срока.
Электронная формула
Оставим на время в стороне вещества, которые взаимодействуют с бромной водой, и посмотрим на строение атома Br. При массовом числе 80 у него 4 орбиты, по которым вокруг ядра вращаются 35 электронов. Также у него есть 45 нейтронов и 35 протонов.
Распределение можно записать так:
История открытия
Сам Br был впервые описан в 1826 году Антуаном Баларом – препаратором из Монпелье. Молодой ученый получил темно-бурую жидкость из сожженных морских водорослей и назвал ее муридом (по аналогии с латинским muria, то есть «рассол»). Хотя немногим раньше, в 1825м, ассистент профессора Гмелина, студент Левиг с помощью хлора выделил элемент из кройцнахского источника. Правда, пока немец собирал достаточное количество материала для проведения исследований, француз его опередил, заявив о своем открытии.
В любом случае заседатели специально собранной комиссии (среди которых был и знаменитый Гей-Люссак) из Парижской академии наук посовещались и признали название Балара неудачным. Дело в том, что в то время семейству солей хлороводородной кислоты было дано имя муриаты. Вот ученые и посчитали, что слишком созвучные термины вызовут путаницу, и вместо этого предложили вариант Brome (с греческого переводится как «зловонный»), потому что открытие неприятно пахло. Его и ввели в употребление по всему миру, естественно, с поправкой на языковые особенности.
Приготовление бромной воды: получение, применение, цвет
Сначала – несколько слов о самом Br. При стабильно комнатной температуре он является жидким (и это единственный неметалл с таким состоянием) и обладает теми же характеристиками, что и галогены. По своей реакционной способности он находится между хлором и йодом. Визуально он тягучий и красно-коричневый, прямо как NO2, но спутать их невозможно из-за запаха, ярко выраженного и негативно воспринимаемого обонянием.
Элемент повсеместно распространен и сегодня, причем наивысшее его содержание фиксируется в соленых озерах и морях (откуда он может попадать и в пресные источники). За счет более высокой плотности бром растворяется в воде очень легко, делая ее оранжевой.
Есть два способа приготовления – рассмотрим каждый. Согласно первому методу, нужно:
При всей кажущейся простоте действия важно соблюдать предельную осторожность и работать только в защитной одежде и в вытяжном шкафу. Все потому, что при соединении двух компонентов выделяются ядовитые испарения.
Более безопасный, а значит и удобный вариант – расщепление порошка NaBr и помощью отбеливателя (с хлором, но без добавок и ароматизаторов) и HCl. Происходит следующим путем:
Чем отличается бромная вода от брома: состав
Растворяясь, рассматриваемый нами элемент запускает реакции оксидации, которые приводят к диспропорциональному выделению бромида и гипобромита – в соответствии с представленной ниже закономерностью:
Br2 + H2O → BrO- + Br- + 2H+
Это продолжается таким же неравным образованием бромата и бромида – следующим образом:
3Br2 + 6OH → BrO3- + 5 Br- + 3H2O
Поведение присутствующих кислот определяет условия хранения. Содержать данный продукт необходимо в затемненной стеклянной посуде и не вынося на свет. Если пренебречь этими правилами и поднести жидкость под прямые солнечные лучи (или в тепло), это спровоцирует выделение кислорода. Что происходит с бромной водой в этом случае? Она не только теряет свои полезные характеристики, но и начинает испускать газ HBr, пары которого ядовиты и очень неприятно пахнут.
| Соединение, функциональная группа | Реагент | Что наблюдается, уравнение реакции |
| Светло-желтая окраска разбавленного раствора соли трехвалентного железа сменяется на фиолетовую | ||
| Анилин | Бромная вода | |
| Любая сильная неорганическая кислота или кислота средней силы H2SO4 (разб.) HCl HI HBr HNO3 (разб.) H3PO4 |